Výskumníci z UC Riverside urobili bezprecedentný prielom v liečbe rakoviny tým, že vyvinuli peptid, ktorý dokáže regulovať MYC, kľúčový proteín podieľajúci sa na väčšine ľudských rakovín. Táto inovácia ponúka novú nádej na zameranie sa na rakovinu na molekulárnej úrovni, čím pripravuje pôdu pre účinnejšiu liečbu.
Objav otvára cestu pre účinnejšiu liečbu.
Zoznámte sa s MYC, beztvarým proteínom zodpovedným za zhoršenie väčšiny prípadov ľudskej rakoviny. Výskumníci z UC Riverside našli spôsob, ako to obmedziť a ponúknuť nádej na novú éru liečby.
V zdravých bunkách pomáha MYC riadiť proces transkripcie, pri ktorom sa prekladá genetická informácia. dna In kráľovská armáda A nakoniec v bielkovinách. „Za normálnych okolností je aktivita MYC prísne regulovaná. V rakovinových bunkách sa stáva nadmerne aktívnym a nie je správne regulovaný,“ povedal Min Zou, docent chémie UCR.
„MYC je menej ako potrava pre rakovinové bunky a skôr ako steroid, ktorý podporuje rýchly rast rakoviny,“ povedal Zou. „To je dôvod, prečo je MYC vinníkom v 75% všetkých prípadov rakoviny u ľudí.“
Na začiatku tohto projektu výskumný tím UCR veril, že ak by dokázali znížiť aktiváciu MYC, mohli by otvoriť okno, v ktorom by bolo možné kontrolovať rakovinu.
Nájsť spôsob, ako kontrolovať MYC, však bolo náročné, pretože na rozdiel od väčšiny iných proteínov MYC nemá žiadnu štruktúru. „Je to v podstate sféra náhodnosti,“ povedal Zou. „Tradičné kanály na objavovanie liekov sa spoliehajú na dobre definované štruktúry a to pre MYC neexistuje.“
Inovatívne prístupy k objavovaniu liekov
Pribudol nový papier Journal of the American Chemical SocietyŠtúdia, ktorej hlavným autorom je Zou, opisuje peptidovú zlúčeninu, ktorá sa viaže na MYC a potláča jej aktivitu.
V roku 2018 výskumníci zistili, že zmena tuhosti a tvaru peptidu zlepšuje jeho schopnosť interagovať s neštruktúrovanými proteínovými cieľmi, ako je MYC.
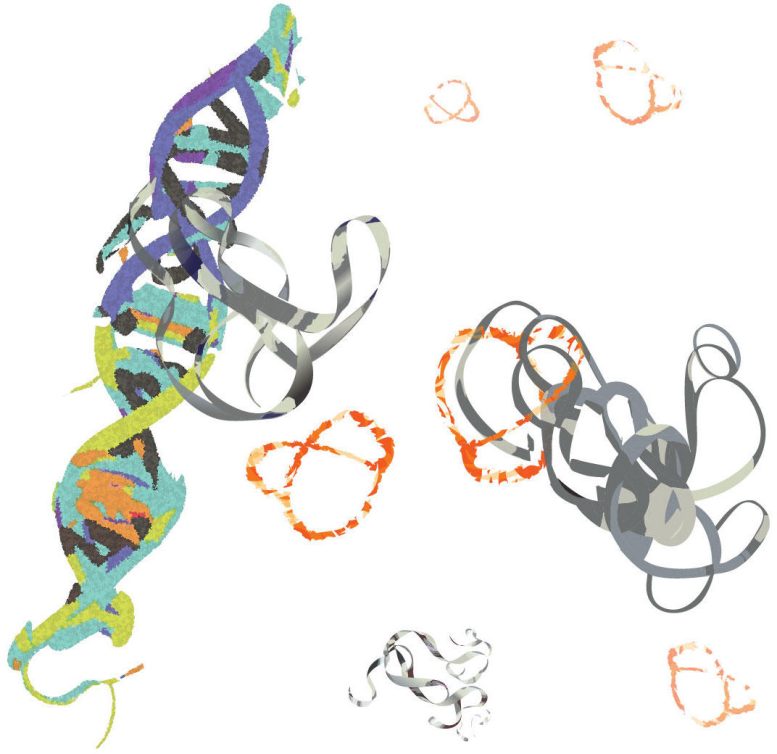
Proteíny MYC (sivá stuha) sa viažu na DNA a podporujú progresiu rakoviny. Výskumníci UCR vyvinuli molekulu (v tvare oranžového praclíka), ktorá sa viaže na MYC a blokuje jej funkciu podporujúcu rakovinu. Kredit: Min Zou/UCR
„Peptidy môžu mať rôzne formy, tvary a polohy,“ povedal Zou. „Keď ich ohnete a spojíte, aby vytvorili prstence, nemôžu nadobudnúť iné možné formy, takže majú nízku úroveň náhodnosti. „Pomáha to pri spájaní.“
Pokroky v poskytovaní liečby a vyhliadky do budúcnosti
V článku tím opisuje nový peptid, ktorý sa viaže priamo na MYC s takzvanou submikromolárnou afinitou, ktorá sa blíži sile protilátky. Inými slovami, je to veľmi silná a špecifická interakcia.
„V porovnaní s predchádzajúcimi verziami sme zlepšili väzbový výkon tohto peptidu až o dva rády,“ povedal Zou. „Tým sa približuje k našim cieľom vývoja liekov.“
V súčasnosti výskumníci používajú lipidové nanočastice na dodanie peptidu do buniek. Sú to malé guľôčky vyrobené z molekúl tuku a nie sú ideálne na použitie ako liek. Výskumníci vyvíjajú chemikáliu, ktorá zlepšuje schopnosť vedúceho peptidu dostať sa do buniek.
Keď sa peptid dostane do bunky, naviaže sa na MYC, čím zmení fyzikálne vlastnosti MYC a zabráni mu vykonávať transkripčné aktivity.
Táto práca je možná čiastočne vďaka financovaniu z Ministerstva obrany USA a medicínskeho výskumu riadeného Kongresom a Národný inštitút zdravia,
Zouovo laboratórium v UC Riverside vyvíja molekulárne nástroje na lepšie pochopenie biológie a využitie týchto znalostí na objavovanie liekov. Dlho sa zaujímal o chémiu chaotických procesov, čo ho pritiahlo k výzve skrotiť MYC.
„MYC v podstate predstavuje chaos, pretože mu chýba štruktúra. To a jeho priamy vplyv na mnohé typy rakoviny z neho robí jednu z najdôležitejších vecí pri vývoji liekov proti rakovine,“ povedal Zou. „Sme veľmi nadšení, že je teraz na dosah.“
Odkaz: „MYC-Targeting Inhibitors Generated from a Stereodiversified Bicyclic Peptide Library“ od Zhonghan Li, Yi Huang, Ta I Hung, Jiannan Sun, Desiree Aispuro, Boxie Chen, Nathan Guevara, Fei Jie, Xu Kang, Lingchao Zhu, Siwen Wang. Zilei Guo, Chia-En Chang a Min Xue, 3. januára 2024, Journal of the American Chemical Society,
DOI: 10.1021/jac.3c09615

Web nerd. Extreme organizer. Writer. Whole foods evangelist. Certified introvert.