zhrnutie: Nový prístup k terapii kmeňovými bunkami odstraňuje zavedené mozgové nádory a poskytuje dlhodobú imunitu trénovaním imunitného systému, aby sa zabránilo návratu rakoviny.
zdroj: Brigham a ženská nemocnica
Vedci používajú nový spôsob, ako premeniť rakovinové bunky na silné protirakovinové látky.
V najnovšej práci z laboratória Khalida Shaha, MS, PhD, v Brigham and Women’s Hospital, zakladajúceho člena Mass General Brigham Healthcare System, výskumníci vyvinuli nový prístup k bunkovej terapii na eradikáciu zavedených nádorov a indukciu dlhších . Termín imunita, tréning imunitného systému, aby sa zabránilo opakovaniu rakoviny.
Tím testoval svoju dvojúčinnú vakcínu zabíjajúcu rakovinu na pokročilom myšom modeli smrteľného glioblastómu rakoviny mozgu so sľubnými výsledkami.
Zistenia boli zverejnené v r veda translačná medicína,
„Náš tím sa riadil jednoduchou myšlienkou: vziať rakovinové bunky a premeniť ich na zabijaky rakoviny a vakcíny,“ povedal zodpovedajúci autor Khalid Shah, MS, PhD, riaditeľ Centra pre kmeňové bunky a translačnú imunoterapiu (CSTI). podpredsedníčka výskumu na oddelení neurochirurgie v Brighame a na fakulte Harvardskej lekárskej fakulty a Harvardského inštitútu kmeňových buniek (HSCI).
„Pomocou génového inžinierstva preprogramujeme rakovinové bunky, aby sme vyvinuli liečivo, ktoré zabíja nádorové bunky a stimuluje imunitný systém, aby zničil primárny nádor a zabránil rakovine.“
Vakcíny proti rakovine sú aktívnou oblasťou výskumu mnohých laboratórií, ale prístup, ktorý zvolili Shah a jeho kolegovia, je odlišný. Namiesto použitia inaktivovaných nádorových buniek sa tím preprogramoval na živé nádorové bunky, ktoré majú nezvyčajnú charakteristiku. Rovnako ako poštové holuby, prežívajúce nádorové bunky precestujú veľké vzdialenosti cez mozog, aby sa vrátili na miesto svojich nádorových buniek.
Shahov tím s využitím tejto jedinečnej vlastnosti skonštruoval živé nádorové bunky pomocou nástroja na úpravu génov CRISPR-Cas9 a preprogramoval ich tak, aby uvoľnili činidlo zabíjajúce nádorové bunky.
Okrem toho boli skonštruované nádorové bunky navrhnuté tak, aby exprimovali faktory, ktoré uľahčujú imunitnému systému ich prioritizáciu, označenie a zapamätanie predĺženej protinádorovej reakcie.
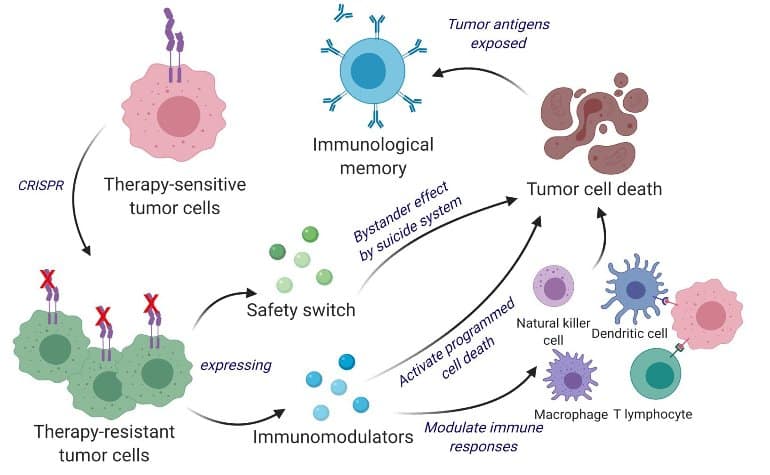
Tím testoval svoje zrekonštruované CRISPR-vylepšené a reverzne skonštruované terapeutické nádorové bunky (ThTC) v rôznych kmeňoch myší, vrátane buniek kostnej drene, pečene a týmusu odvodených od ľudí, aby napodobnili ľudské imunitné mikroprostredie. Shahov tím tiež vytvoril dvojúrovňový bezpečnostný spínač v rakovinovej bunke, ktorý po aktivácii vymaže ThTC, keď sú potrebné.
Táto bunková terapia s dvojitým účinkom bola v týchto modeloch bezpečná, použiteľná a účinná, čo naznačuje plán k terapii. Zatiaľ čo je potrebné ďalšie testovanie a vývoj, Shahov tím si konkrétne vybral tento model a použitie ľudských buniek na vyhladenie cesty na preloženie ich zistení do nastavení pacienta.
„Počas práce, ktorú robíme v centre, aj keď je vysoko technická, nikdy nestratíme pacienta z dohľadu,“ povedal Shah.
„Naším cieľom je zaujať inovatívny, no translačný prístup, aby sme mohli vyvinúť terapeutickú vakcínu zabíjajúcu rakovinu, ktorá bude mať v medicíne v konečnom dôsledku trvalý vplyv.“
Shah a kolegovia poznamenávajú, že táto terapeutická stratégia je použiteľná na širokú škálu solídnych nádorov a je potrebné ďalšie skúmanie jej aplikácií.
O týchto novinkách z výskumu rakoviny mozgu
autor: Tlačové oddelenie
zdroj: Brigham a ženská nemocnica
Kontakt: Tlačové oddelenie – Brigham and Women’s Hospital
obrázok: Obrázok je pripísaný Kok Siong Chen a Khalid Shah
Základný výskum: otvorený prístup.
,Bifunkčná vakcína na báze rakovinových buniek súčasne riadi priame zabíjanie nádorov a protinádorovú imunituKok-seong Chen a kol. veda translačná medicína
zhrnutie
Bifunkčná vakcína na báze rakovinových buniek súčasne riadi priame zabíjanie nádorov a protinádorovú imunitu
Je známe, že podávanie inaktivovaných nádorových buniek indukuje silnú protinádorovú imunitnú odpoveď; Účinnosť takýchto prístupov je však obmedzená ich neschopnosťou zabiť nádorové bunky pred vyvolaním imunitných reakcií. Na rozdiel od spiacich nádorových buniek majú živé nádorové bunky schopnosť sledovať a zameriavať sa na nádory.
Tu sme vyvinuli terapeutikum na báze celých rozvetvených rakovinových buniek s priamym zabíjaním nádorov a imunostimulačnými úlohami. Nádorové bunky citlivé na interferón-β (IFN-β) sme preprogramovali tak, aby boli voči nim rezistentné vyradením IFN-β-špecifického receptora pomocou CRISPR-Cas9 a následne sme ich vystavili imunomodulačnému činidlu IFN-β a granulocytovo-makrofágovej kolónii- tvoriace činidlo (IFN-β).Vyvinuté na uvoľňovanie stimulujúcich faktorov. ,
Tieto skonštruované terapeutické nádorové bunky (ThTC) eliminovali zavedené glioblastómové nádory u myší indukciou apoptózy rakovinových buniek sprostredkovanej kaspázou, upreguláciou receptora β rastového faktora odvodeného od doštičiek exprimovaného z fibroblastov a protinádorovými imunitnými bunkami aktivovaného prenosu a antigén-špecifického . Signalizácia aktivácie T buniek.
Táto účinnosť ThTC založená na mechanizme sa premietla do výhody prežitia a dlhodobej imunity v modeloch primárnej, recidivujúcej a metastatickej rakoviny u imunokompetentných a humanizovaných myší. Zahrnutie dvojitého zabíjacieho spínača obsahujúceho tymidínkinázu vírusu herpes simplex-1 a kaspázu 9 aktivovanú rapamycínom do ThTC zaistilo bezpečnosť nášho prístupu.
Vytvorenie prirodzene sa vyskytujúcich vznikajúcich nádorových buniek obohatených biofunkčnými terapeutikami predstavuje sľubnú bunkovú imunoterapiu pre solídne nádory a vytvára cestu ku klinickej translácii.

Web nerd. Extreme organizer. Writer. Whole foods evangelist. Certified introvert.

