Vedci navrhujú úplne novú periodickú tabuľku a je to výlet
Periodická tabuľka prvkov, predovšetkým vytvorená ruským chemikom, Dmitrij Mendelejev (1834-1907), oslávil svoje 150. výročie minulý rok. Bolo by ťažké preceňovať jeho význam ako organizačného princípu v chémii – všetci začínajúci chemici sa s ním oboznámia od najskorších etáp svojho vzdelávania.
Vzhľadom na dôležitosť tabuľky by sa dalo odpustiť, ak si myslíme, že usporiadanie prvkov už nebolo predmetom diskusie. Dvaja vedci v Moskve v Rusku však nedávno zverejnili a návrh na novú objednávku.
Najprv zvážime, ako bola vyvinutá periodická tabuľka. Na konci 18. storočia mali chemici jasno v rozdiele medzi prvkom a zlúčeninou: prvky boli chemicky nedeliteľné (príkladmi sú vodík, kyslík), zatiaľ čo zlúčeniny pozostávali z dvoch alebo viacerých prvkov v kombinácii, ktoré mali vlastnosti celkom odlišné od ich zložiek.
Na začiatku 19. storočia tu bola dobrý nepriamy dôkaz pre existenciu atómov. A v šesťdesiatych rokoch 19. storočia bolo možné uviesť známe prvky v poradí podľa ich relatívnej atómovej hmotnosti – napríklad vodík bol 1 a kyslík 16.
Jednoduché zoznamy majú samozrejme jednorozmerný charakter. Chemici si však boli vedomí, že určité prvky majú dosť podobné chemické vlastnosti: napríklad lítium, sodík a draslík alebo chlór, bróm a jód.
Zdalo sa, že sa niečo opakuje a položením chemicky podobných prvkov vedľa seba sa dal zostrojiť dvojrozmerný stôl. Zrodila sa periodická tabuľka.
Dôležité je, že Mendelejevova periodická tabuľka bola odvodená empiricky na základe pozorovaných chemických podobností určitých prvkov. Až začiatkom 20. storočia, po založení štruktúry atómu a po vývoji kvantovej teórie, dôjde k teoretickému pochopeniu jeho štruktúry.
Prvky boli teraz usporiadané podľa atómového čísla (počet kladne nabitých častíc nazývaných protóny v atómovom jadre), a nie podľa atómovej hmotnosti, ale stále tiež podľa chemických podobností.
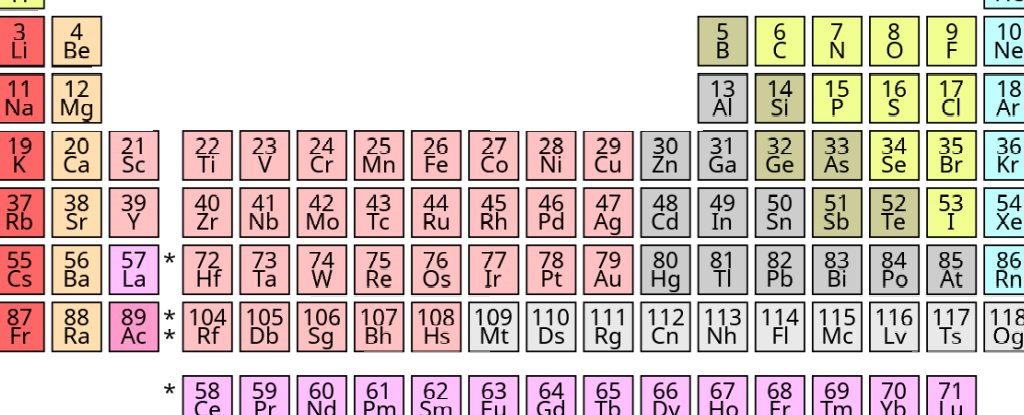
To ale teraz vyplývalo z usporiadania elektrónov opakujúcich sa v takzvaných „škrupinách“ v pravidelných intervaloch. Do 40. rokov 20. storočia väčšina učebníc obsahovala periodickú tabuľku podobnú tej, ktorú vidíme dnes, ako je to znázornené na obrázku nižšie.
Dnešná periodická tabuľka. (Offnfopt / Wikipedia)
Bolo by pochopiteľné myslieť si, že by to bol koniec veci. Nie však tak. Jednoduché vyhľadávanie na internete odhalí všetky druhy verzií periodickej tabuľky.
Existujú krátke verzie, dlhé verzie, kruhové verzie, špirálové verzie a dokonca aj trojrozmerné verzie. Mnohé z nich, samozrejme, sú jednoducho rôzne spôsoby prenosu tých istých informácií, naďalej však panujú nezhody v otázkach, kam by sa niektoré prvky mali umiestniť.
Presné umiestnenie určitých prvkov závisí od toho, ktoré konkrétne vlastnosti chceme zvýrazniť. Periodická tabuľka, ktorá dáva prednosť elektronickej štruktúre atómov, sa teda bude líšiť od tabuliek, pre ktoré sú základnými kritériami určité chemické alebo fyzikálne vlastnosti.
Tieto verzie sa príliš nelíšia, ale existujú určité prvky – napríklad vodík -, ktoré by sme mohli umiestniť celkom odlišne podľa konkrétnej vlastnosti, ktorú by sme chceli zdôrazniť. Niektoré tabuľky umiestňujú vodík do skupiny 1, zatiaľ čo v iných sa nachádza na vrchole skupiny 17; niektoré stoly ju dokonca majú v skupine samostatne.
Oveľa radikálnejšie však môžeme zvážiť usporiadanie prvkov veľmi odlišným spôsobom, ktorý nezahŕňa atómové číslo alebo odráža elektronickú štruktúru – a vrátime sa k jednorozmernému zoznamu.
Nový návrh
Posledný pokus o objednávanie prvkov týmto spôsobom bol nedávno uverejnený v Journal of Physical Chemistry vedcami Zahed Allahyari a Artem Oganov.

Ich prístup, stavať na skoršej práci iných, je priradiť každému prvku to, čo sa nazýva Mendeleevovo číslo (MN).
Existuje niekoľko spôsobov, ako odvodiť takéto čísla, ale najnovšia štúdia používa kombináciu dvoch základných veličín, ktoré je možné merať priamo: atómový polomer prvku a vlastnosť tzv. elektronegativita ktorý popisuje, ako silno atóm priťahuje k sebe elektróny.
Ak si niekto objedná prvky podľa svojich MN, majú najbližší susedia, prekvapivo, dosť podobné MN. Ale ešte užitočnejšie je urobiť tento krok o krok ďalej a skonštruovať dvojrozmernú mriežku založenú na MN prvkov, ktoré tvoria prvky v takzvaných „binárnych zlúčeninách“.
Jedná sa o zlúčeniny zložené z dvoch prvkov, ako je chlorid sodný, NaCl.
Aká je výhoda tohto prístupu? Dôležité je, že môže pomôcť predpovedať vlastnosti binárnych zlúčenín, ktoré ešte neboli vyrobené. To je užitočné pri hľadaní nových materiálov, ktoré sú pravdepodobne potrebné pre budúce aj existujúce technológie. Nepochybne sa to časom rozšíri na zlúčeniny s viac ako dvoma elementárnymi zložkami.
Dobrý príklad dôležitosti hľadania nových materiálov možno oceniť zvážením periodickej tabuľky zobrazenej na obrázku nižšie.

Táto tabuľka ilustruje nielen relatívne veľké množstvo prvkov (čím je políčko pre každý prvok väčšie, tým je ich viac), ale tiež upozorňuje na potenciálne problémy s dodávkami súvisiace s technológiami, ktoré sa stali všadeprítomnými a nevyhnutnými v našom každodennom živote.
Zoberme si napríklad mobilné telefóny. Všetky prvky použité pri ich výrobe sú označené ikonou telefónu a môžete vidieť, že niekoľkých požadovaných prvkov je stále menej – ich budúca ponuka je neistá.
Ak máme vyvinúť náhradné materiály, ktoré sa vyhýbajú použitiu určitých prvkov, poznatky získané pri objednávaní prvkov podľa ich MN sa môžu pri tomto hľadaní ukázať ako cenné.
Po 150 rokoch vidíme, že periodické tabuľky nie sú iba životne dôležitým vzdelávacím nástrojom, pre výskumníkov zostávajú užitočné pri hľadaní základných nových materiálov. Nemali by sme si však myslieť, že nové verzie budú náhradou za staršie vyobrazenia. Mnoho rôznych tabuliek a zoznamov slúži iba na prehĺbenie nášho chápania toho, ako sa prvky správajú.
Nick Norman, Profesor chémie, Univerzita v Bristole.
Tento článok je publikovaný od Konverzácia na základe licencie Creative Commons. Čítať pôvodný článok.

Web nerd. Organizátor extrémov. Spisovateľ. Evanjelista celkom potravín. Certifikovaný introvert.